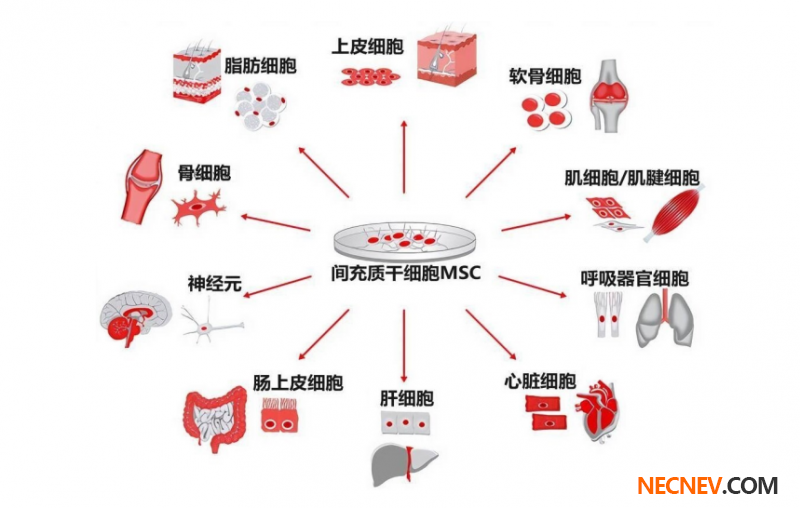
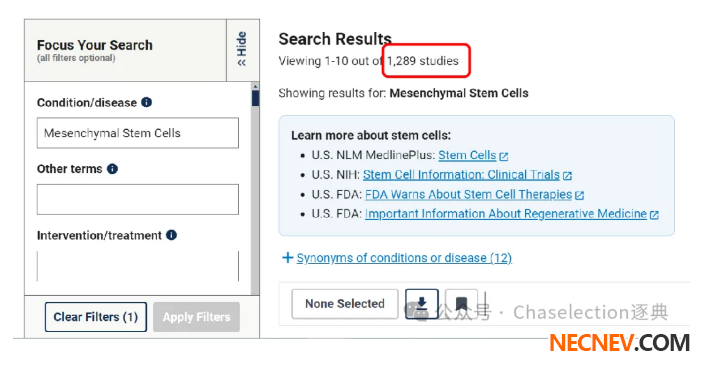
据ClinicalTrials.gov临床注册数据显示,目前全球范围内与MSCs相关临床试验多达1300项。MSCs已成为当今医学研究领域最前沿、最热门的方向之一,未来发展潜力巨大。
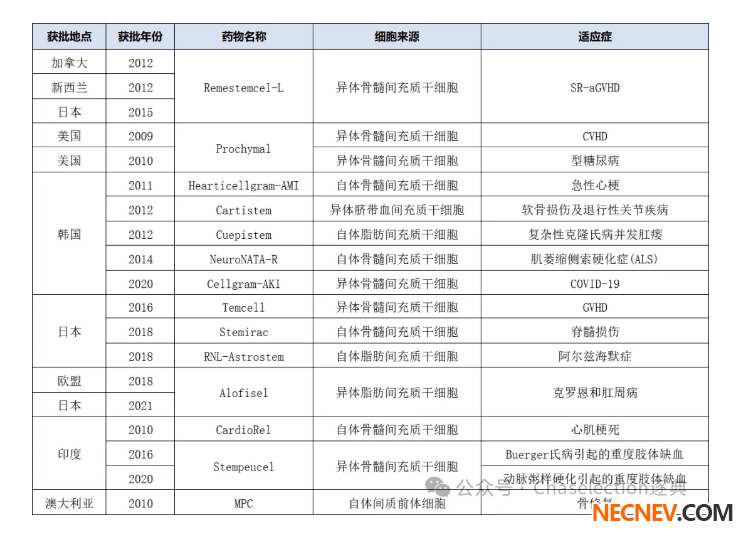
在国内利好政策环境的推动,干细胞产业市场规模随之也在迅速扩大。截至2023年7月,我国已有35款MSCs药物共获得近60个IND批件,涉及20多种适应症,其中研究较多的适应症包括移植物抗宿主病、膝骨关节炎、间质性肺病及急性呼吸窘迫综合症等。全球目前也已有14款批准上市的间充质干细胞产品。
MSCs相关药物研发如火如荼,那如何提高MSCs扩增效率,增加细胞活率也随之成为重点关注问题,自然细胞培养各阶段所涉及相关试剂如何选择也成为一大难点,下面以脐带间充质干细胞培养流程为例,探析各环节。
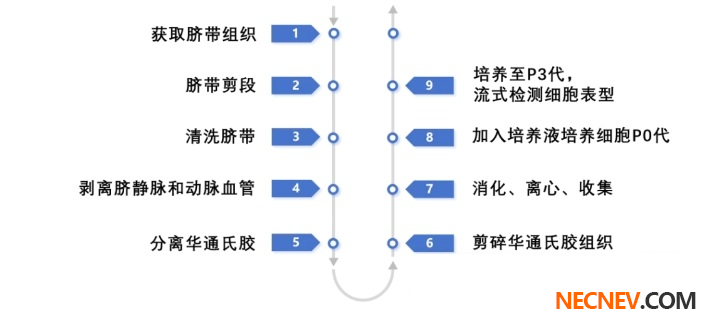
MSCs从人脐带华通氏胶组织获得,经胰酶、胶原酶、分散酶等酶消化、离心、收集得到细胞,选择合适的MSCs培养基培养至P0代,使细胞贴壁生长,而后选取干细胞专用消化液进行细胞传代,培养至P3代即可进行流式检测或细胞表型鉴定。

埃泽思生物携手逐典生物,致力于生命科学技术产业化,为基础研究、细胞治疗、再生医学以及药物发现提供高品质、高性价比的产品与服务。
关于逐典
上海逐典生物科技有限公司,坐落于中国(上海)自由贸易试验区,获得ISO9001质量体系认证,是一家从事重组蛋白研发和销售的高新科技企业。逐典生物始终秉持以客户为中心的理念,针对重组蛋白的结构设计、纯化工艺及其稳定剂型相关的多项关键技术进行优化和突破。专业的定向蛋白变复性技术,可将大肠杆菌大量表达的变性固体蛋白转变成高活性可溶性蛋白。凭借技术优势,逐典生物新品研发周期短且可控性强,为重组蛋白的高质高效研发提供保障,为企业生产降本增效。
关于埃泽思
上海埃泽思生物科技有限公司总部位于上海,公司取名AppliedCell (应用细胞),是一家致力于为细胞治疗、再生医学提供核心原料,以及研发服务(AA CRO) 和细胞药委托开发生产服务(CDMO)的生物科技公司。目前公司产品已经涵盖干细胞、免疫细胞治疗全流程试剂原料。其中核心产品已经完成美国FDA DMF备案以及国家药品评审中心(CDE)药物原辅料备案,是国内资质较为齐全的细胞治疗原料供应商。目前,公司已与国内多家细胞治疗企业进行细胞治疗一类新药联合申报。


